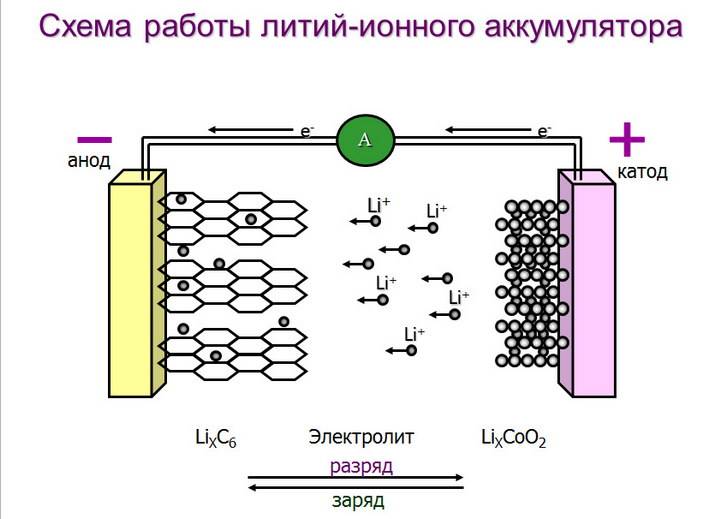
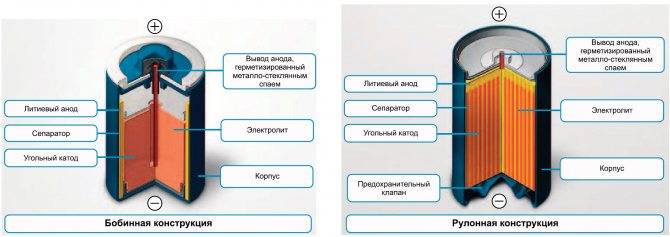
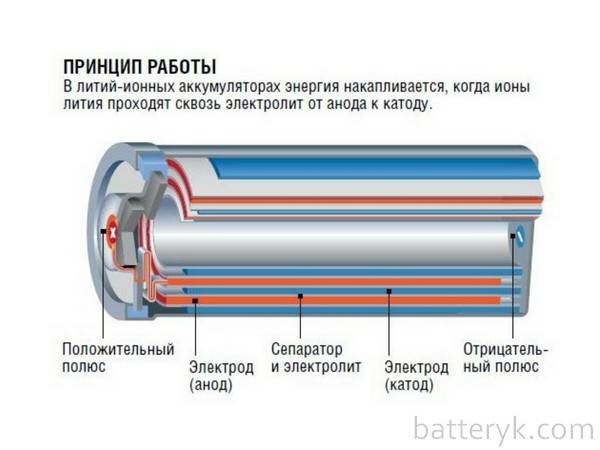
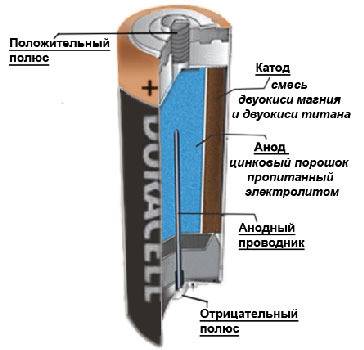
Как устроен литий-ионный аккумулятор?
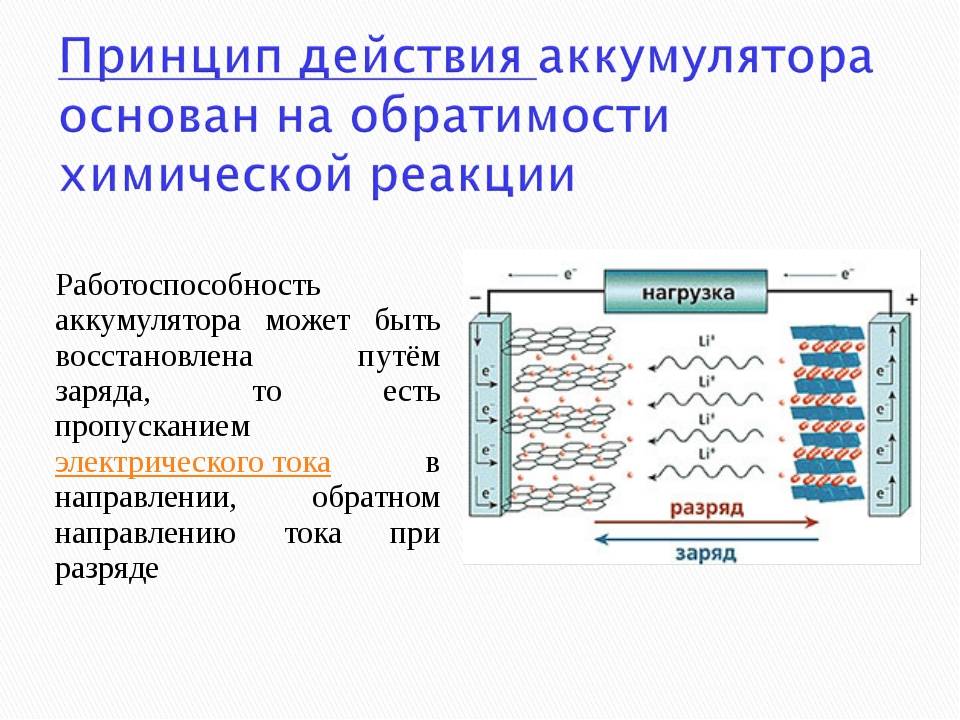
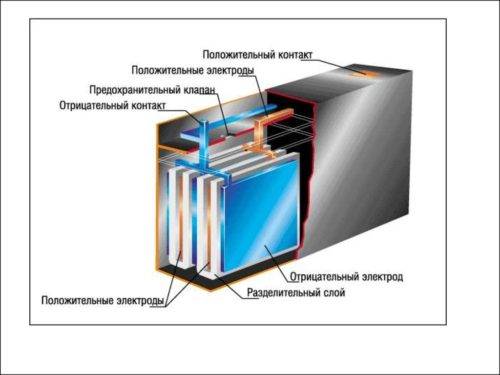
Его конструкция не отличается сложностью: анод из пористого углерода, литиевый катод, пластина-сепаратор между ними и проводник тока – вещество-электролит. Во время разрядки ионы отделяются от анода и движутся на литий по электролиту, минуя сепаратор. Во время питания батареи все происходит с точностью до наоборот – литий отдает ионы, углерод принимает. Так и происходит процесс ионного круговорота между разнозарядными электродами литий-ионной батареи.

Точный состав катода может отличаться в конкретной модели или у определенного производителя АКБ. Дело в том, что многие фирмы тестируют разнообразные типы литиевых соединений для того чтобы изменять показатели устройств по своему усмотрению.
Впрочем, очевидно – улучшая одни характеристики, неизбежно приходится жертвовать другими. Чаще всего литий-ионные АКБ с повышенной емкостью, заботой об эксплуатирующих его людях и природной среде оказываются чрезмерно дорогостоящими или требуют слишком много внимания.
Но чего не отнять у батарей с литием, что составляет их принципиальную разницу с другими типами аккумуляторов, так это низкий уровень саморазряда.
Принципы работы
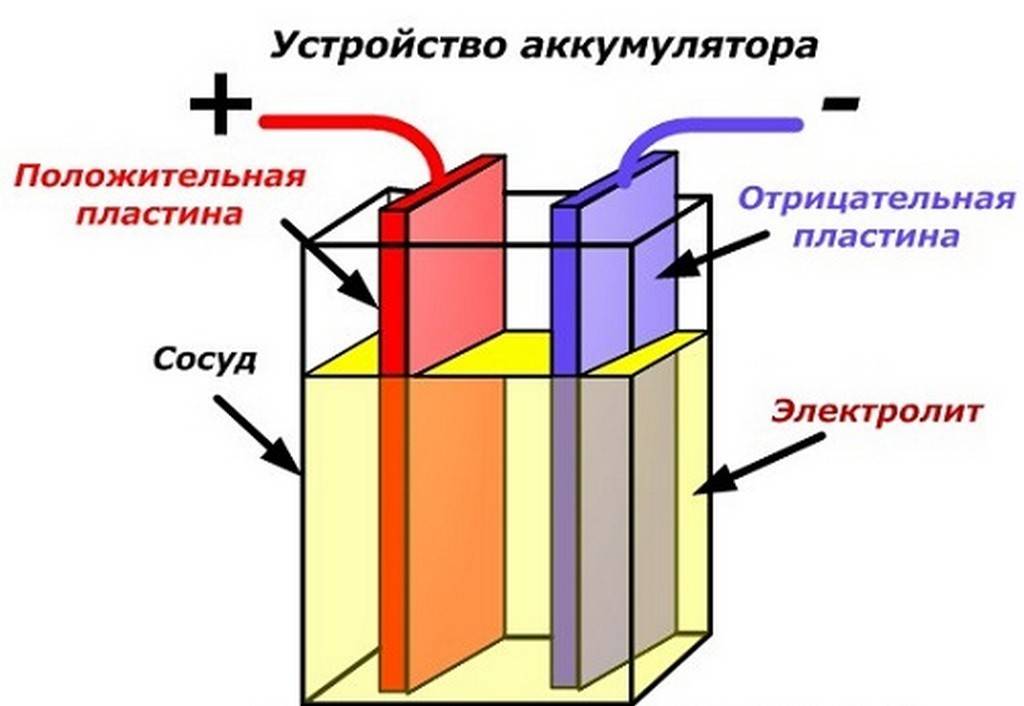
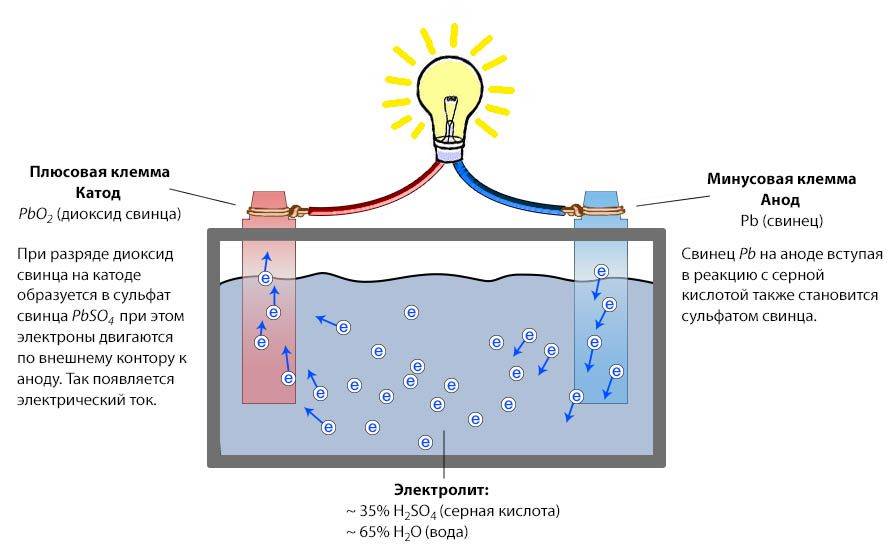
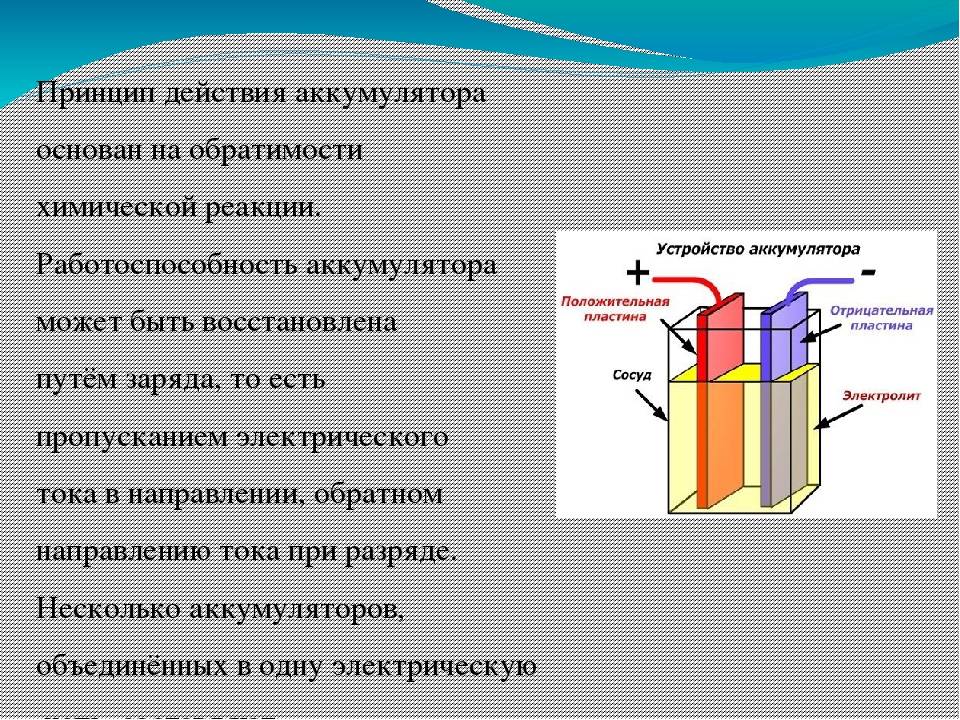
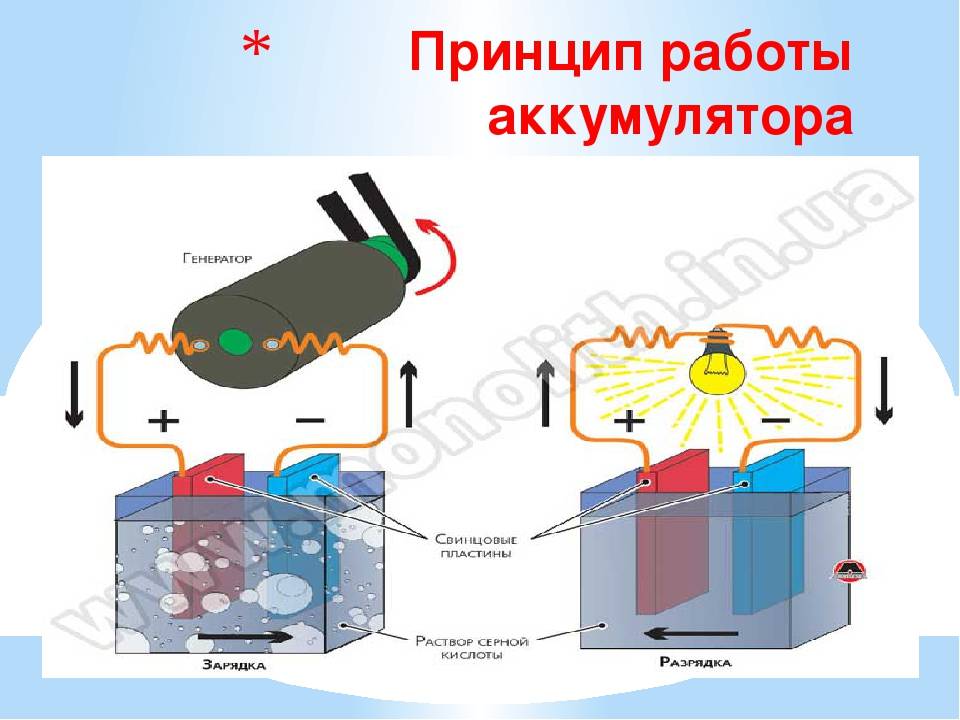
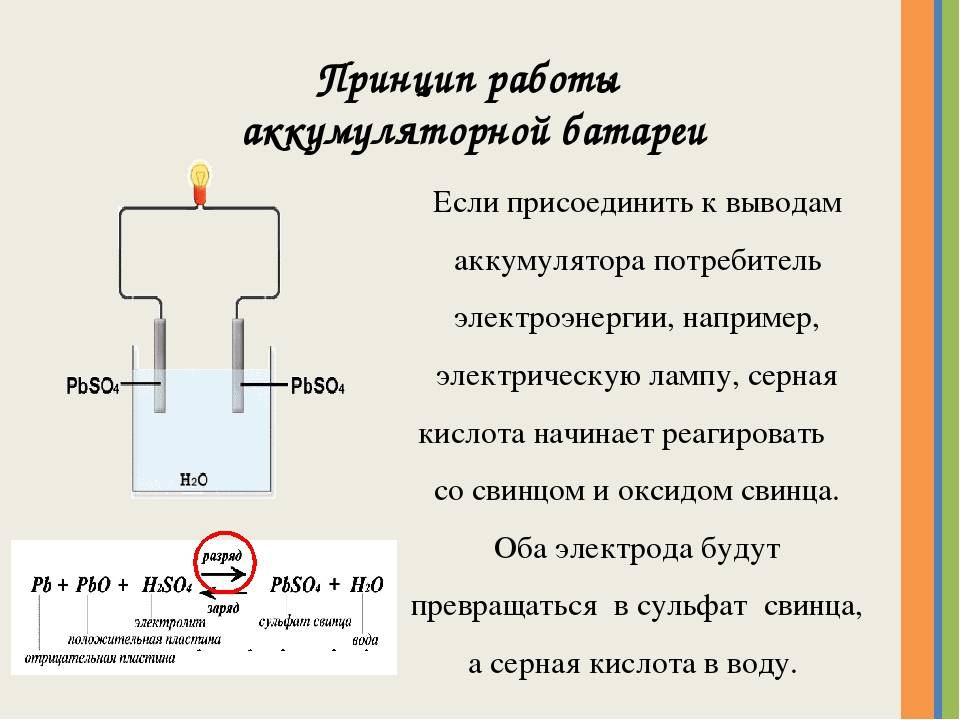
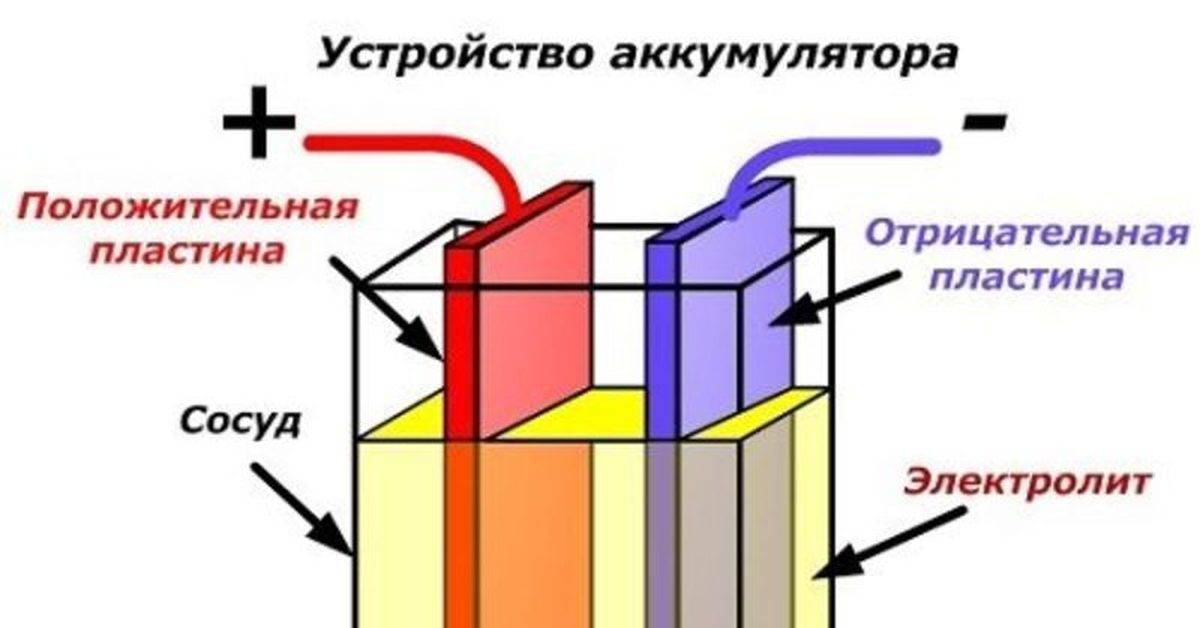
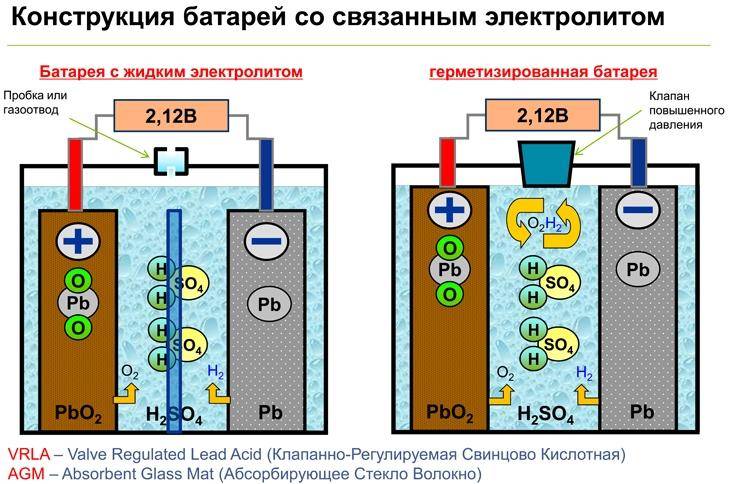
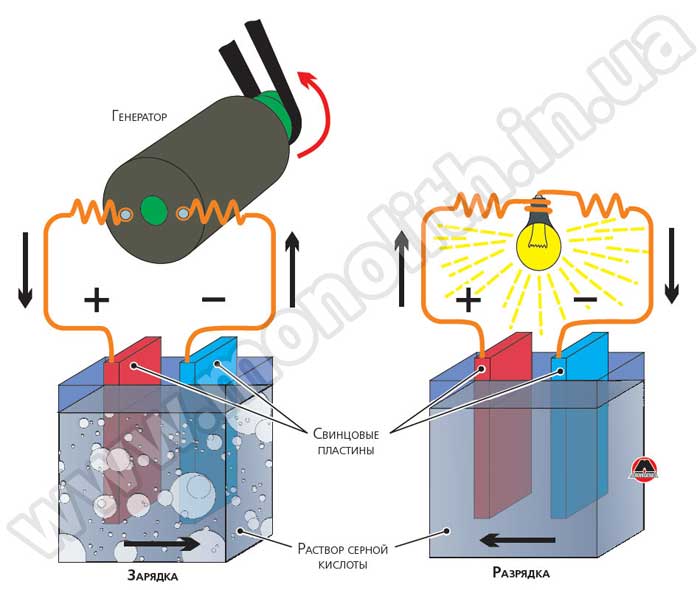
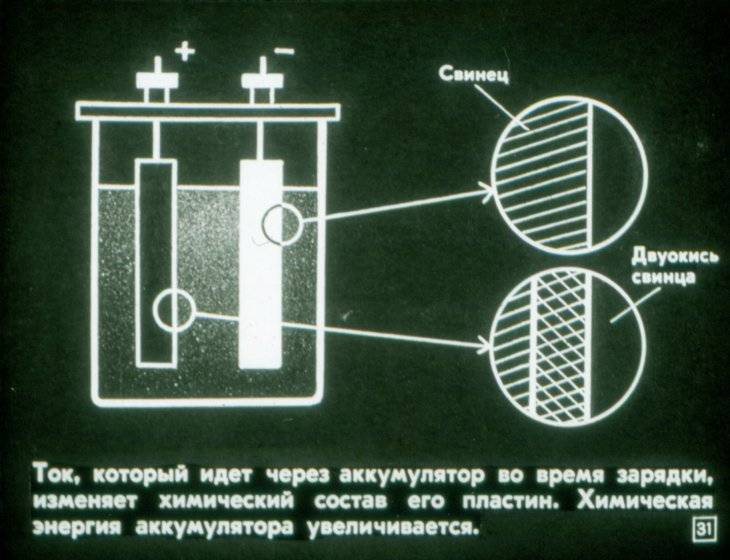
Принцип работы аккумулятора основан на реакции между двуокисью свинца положительной пластины, губчатым свинцом отрицательной пластины и раствором серной кислоты с водой. Этот раствор представляет собой электролит, плотность которого составляет 1,28 г/см3. Происходит образование электрического тока, с одновременным образованием на отрицательной пластине сульфата свинца. Происходит выделение воды из электролита, со снижением его плотности.
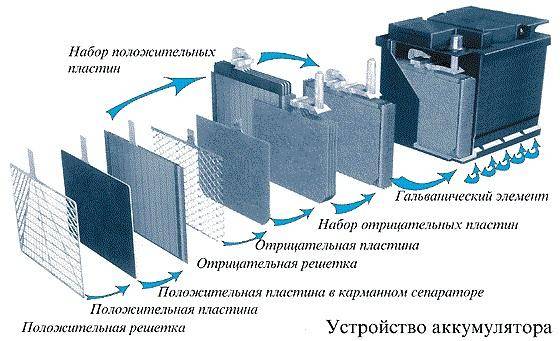
При поступлении электрического тока из внешних источников, таких как генератор или зарядное устройство, электрохимический процесс начинает происходить в обратном направлении. На отрицательных электродах происходит восстановление чистого свинца, а на положительных – регенерируется диоксид свинца. Одновременно повышается плотность электролита.
Таким образом, принцип работы аккумулятора основан на методе двойной сульфатации, позволяющей полностью восстанавливать первоначальные свойства батареи. Срок службы аккумулятора напрямую зависит от качества используемых материалов.
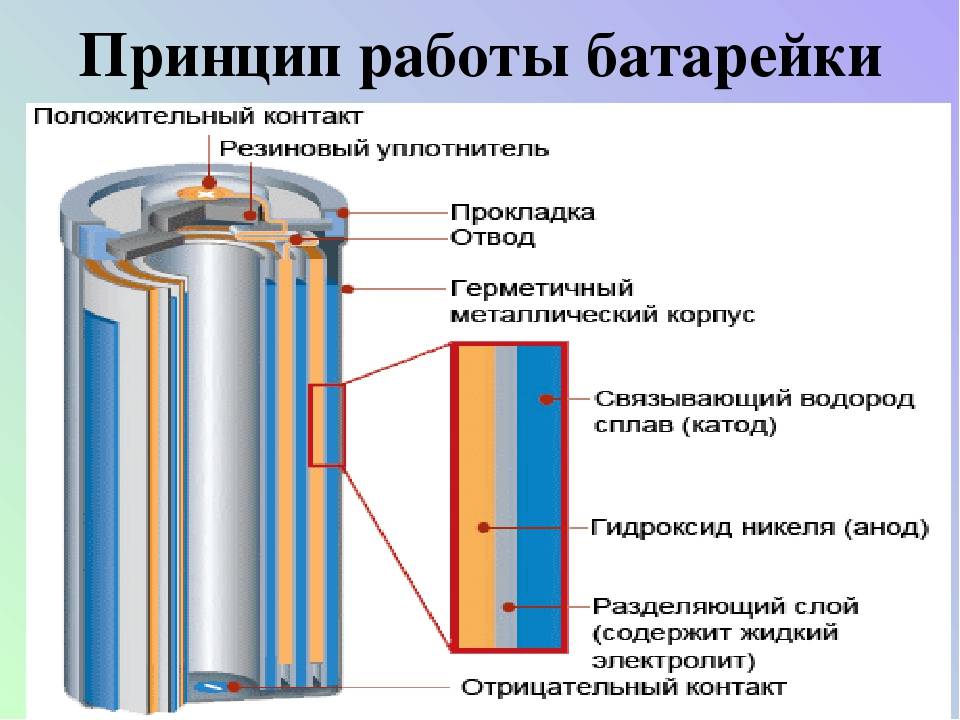
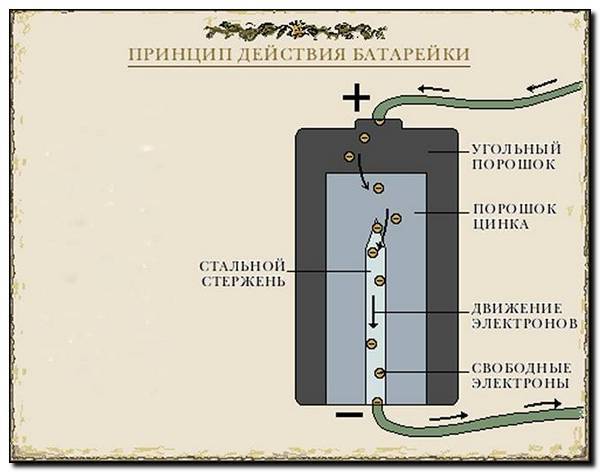
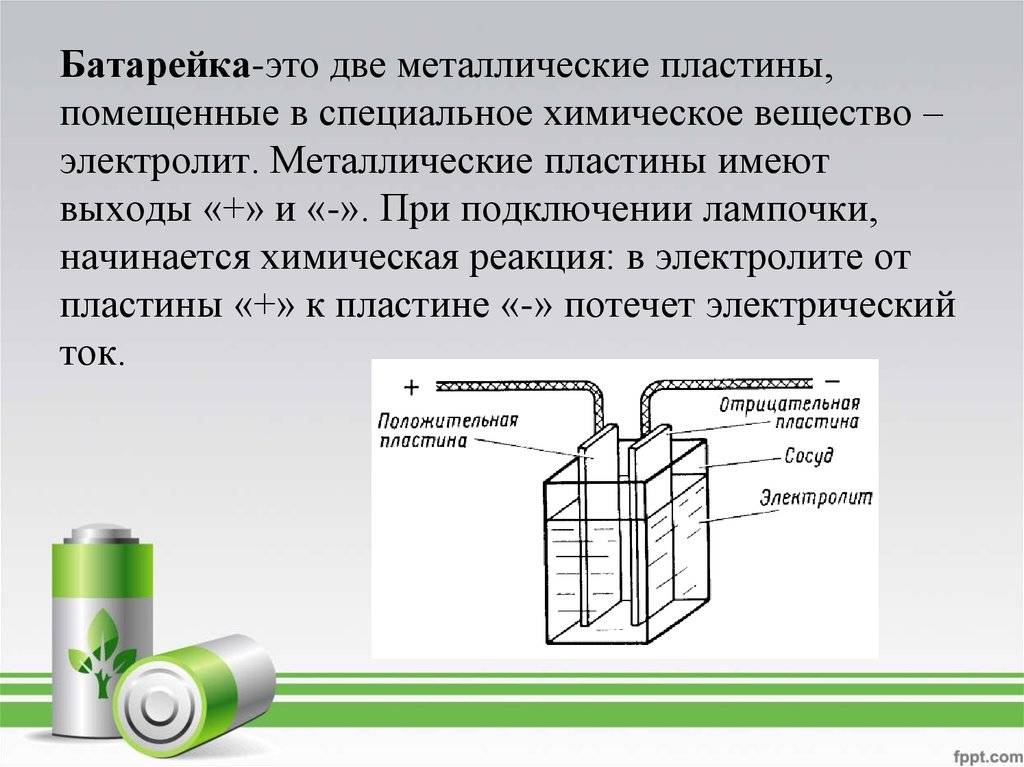
Принцип работы батарейки
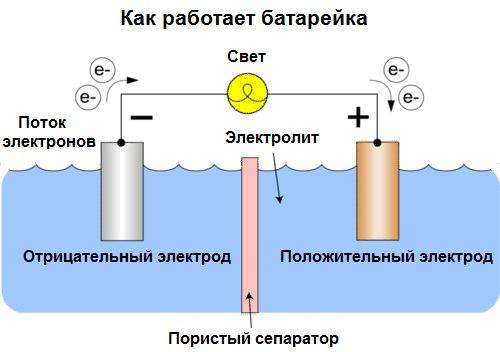
Как работает батарейка
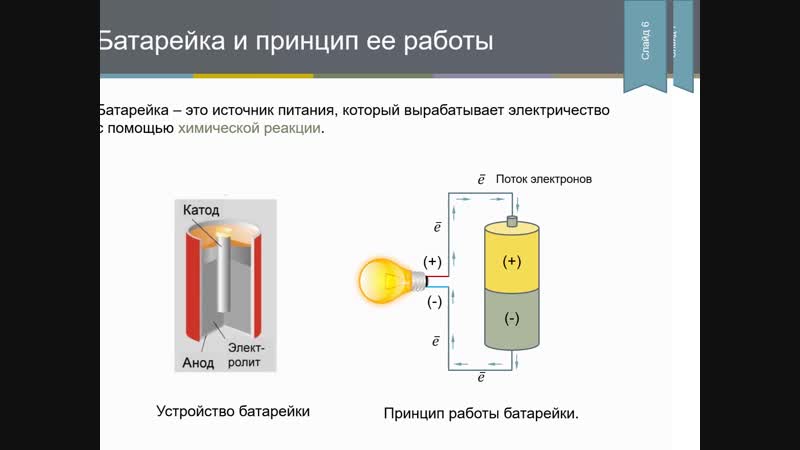
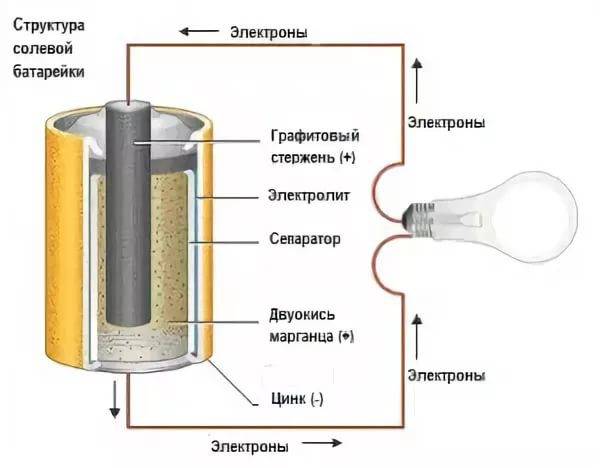
Положительно заряженные частицы двигаются к отрицательным. Средой, где происходит данное движение, является электролит. Заряженные частицы образуются в процессе взаимодействия разных веществ. Весь принцип работы батарейки сводится к химической реакции.
Для прибора необходима нагрузка в виде лампочки или диода, в противном случае при контакте “плюса” и “минуса” может произойти короткое замыкание.
При работе элемента аноды окисляются и разрушаются. Со временем изделие теряет заряд и требует замены. Попытки восстановить его ни к чему хорошему не приведут, т.к. изменения, происходящие в батарее, необратимы.
Если попытаться зарядить конструкцию, то это приведет к взрыву или течи. Но ученым путем проб и ошибок удалось создать восполняемую батарею – аккумулятор.
Химические процессы внутри батарейки
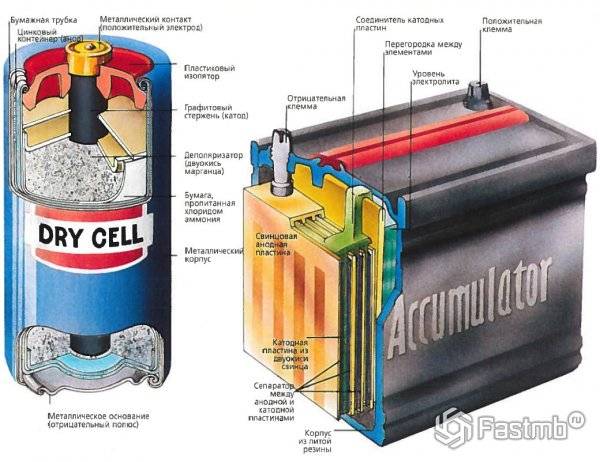
Коротко о происходящем внутри металлического корпуса. Электрические батарейки состоят из двух частей, катода и анода, и жидкости или геля, заполняющего корпус, по совместительству выполняющий роль корпуса и резервуара. Жидкость называется электролитом и обладает некоторой химической активностью. Активность специфическая — электролит забирает электроны на одном полюсе (катод), и отдает их на другой (анод). Там, где избыток электронов, получается заряд «минус», там, где дефицит — «плюс».
По типу электролита и материалов анода и катода, батарейки подразделяются на:
- Солевые. Узнать их можно по маркировке R. Электролит — хлорид аммония. Катод — цинк, анод — кальций. Это самые дешевые батарейки с небольшим запасом работоспособности.
- Щелочные. Маркировка LR. Часто пишут также слово Alkaline. Электролит — гидроксид натрия или калия, катод — цинк, анод — оксид марганца. Обладают средней работоспособностью, но намного лучше солевых. Щелочные батарейки способны создавать напряжение до 12 В, но в быту используются стандартные, на 1,5 В. Так удобнее.
- Литиевые. Маркировка CR. Отличаются тем, что при разной нагрузке выдают стабильный ток. Используются, преимущественно, в точной электронике.
- Серебряные. Маркировка SR. Анод цинковый, катод серебряный. Отличаются высокой емкостью и значительным сроком службы. Используются в дорогой технике, например, хороших наручных часах.
Также выпускаются ртутные батарейки, но по причине токсичности жидкого металла, в бытовой технике практически не используются. Применяются преимущественно в специальных приборах, рассчитанных на эксплуатацию при низких температурах.
Компоновка АКБ
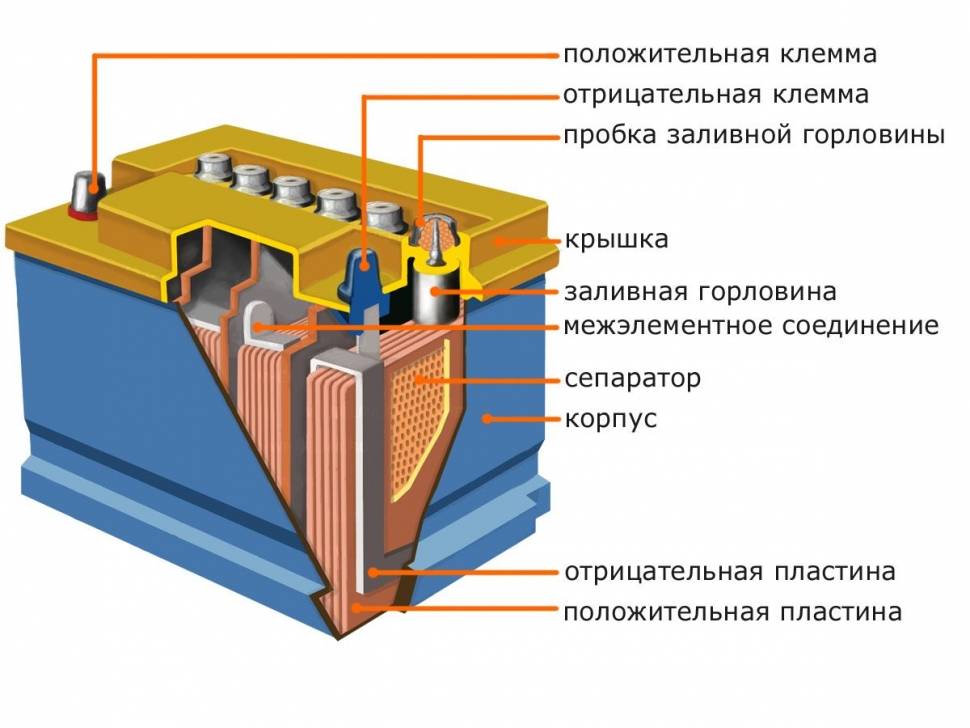
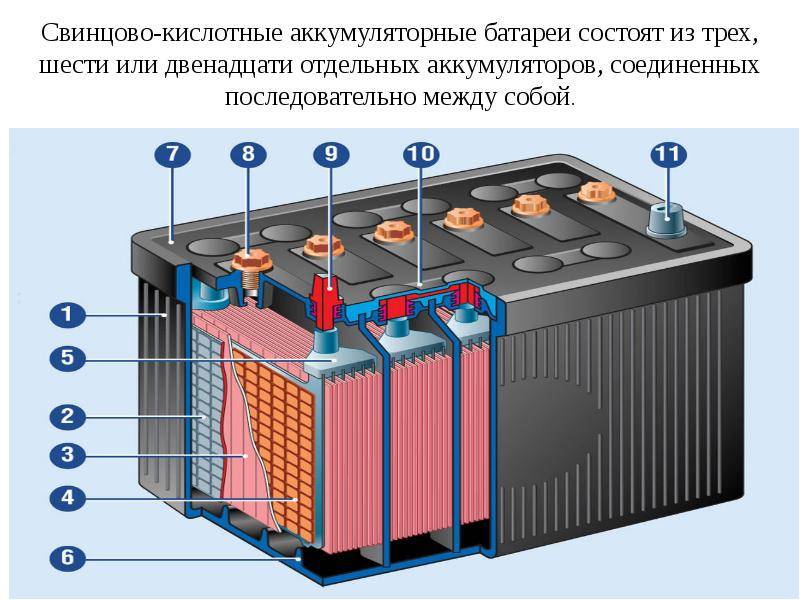
С внешней стороны корпуса такая АКБ имеет элементы, показанные на рисунке ниже.
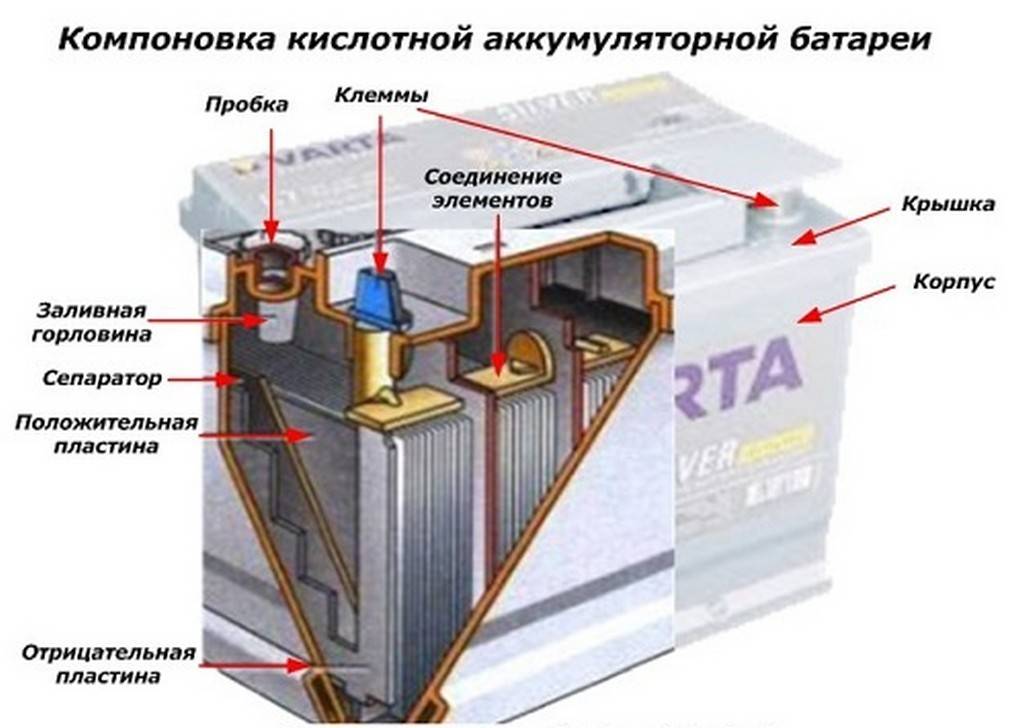 Компоновка кислотной аккумуляторной батареи (АКБ)
Компоновка кислотной аккумуляторной батареи (АКБ)
Из него видно, что прочный пластмассовый корпус закрыт герметично крышкой и сверху оборудован двумя клеммами. Они обычно имеют конусную форму, для подключения к электрической схеме автомобиля. На их выводах выбита маркировка полярности: «+» и «-». При этом есть одно правило: во избежании ошибок при подключении, диаметр положительной клеммы немного больше, чем у отрицательной.
У обслуживаемых аккумуляторных батарей сверху каждой банки помещена заливная горловина, чтобы контролировать уровень электролита либо доливки дистиллированной воды при эксплуатации. В нее вворачиваются пробка, предохраняющая внутренние полости банки от попадания загрязнений и одновременно не дает выливаться электролиту при наклонах АКБ.
Для того, чтобы предотвратить бурное выделение газов из электролита, который возможен при интенсивной езде, в пробках делаются отверстия для предотвращения повышения давления внутри банки. И через эти отверстия выходят кислород и водород, а также пары электролита. Такие ситуации, связанные с чрезмерными токами заряда, желательно избегать.
На том же рисунке выше показано соединение элементов между банками и расположение пластин-электродов.
Стартерные автомобильные АКБ (свинцово-кислотные) работают по принципу двойной сульфатации. На них во время разряда/заряда происходит электрохимический процесс, что сопровождается изменением химического состава активной массы электродов с выделением или поглощением в электролит (серную кислоту) воды.
Этим явлением можно объяснить повышение удельной плотности электролита при заряде, а так же снижение при разряде батареи. Иными словами, величина плотности дает возможность оценивать электрическое состояние АКБ. Для ее замера используют специальный прибор — автомобильный ареометр.
В состав электролита кислотных батарей входит дистиллированная вода. Она же при отрицательной температуре переходит в твердое состояние — лед. Поэтому, чтобы автомобильные аккумуляторы не замерзали в холодное время, необходимо применять специальные меры, предусмотренные правилами эксплуатации.
Принцип работы батарейки
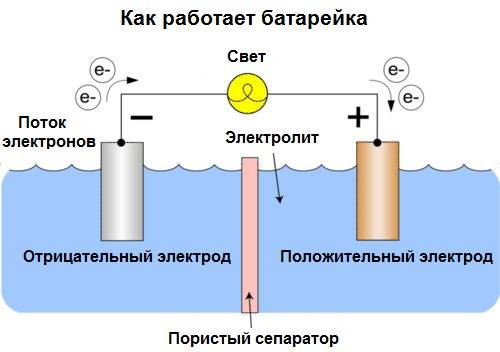
Как работает батарейка
Положительно заряженные частицы двигаются к отрицательным. Средой, где происходит данное движение, является электролит. Заряженные частицы образуются в процессе взаимодействия разных веществ. Весь принцип работы батарейки сводится к химической реакции.
Для прибора необходима нагрузка в виде лампочки или диода, в противном случае при контакте “плюса” и “минуса” может произойти короткое замыкание.
При работе элемента аноды окисляются и разрушаются. Со временем изделие теряет заряд и требует замены. Попытки восстановить его ни к чему хорошему не приведут, т.к. изменения, происходящие в батарее, необратимы.
Если попытаться зарядить конструкцию, то это приведет к взрыву или течи. Но ученым путем проб и ошибок удалось создать восполняемую батарею – аккумулятор.
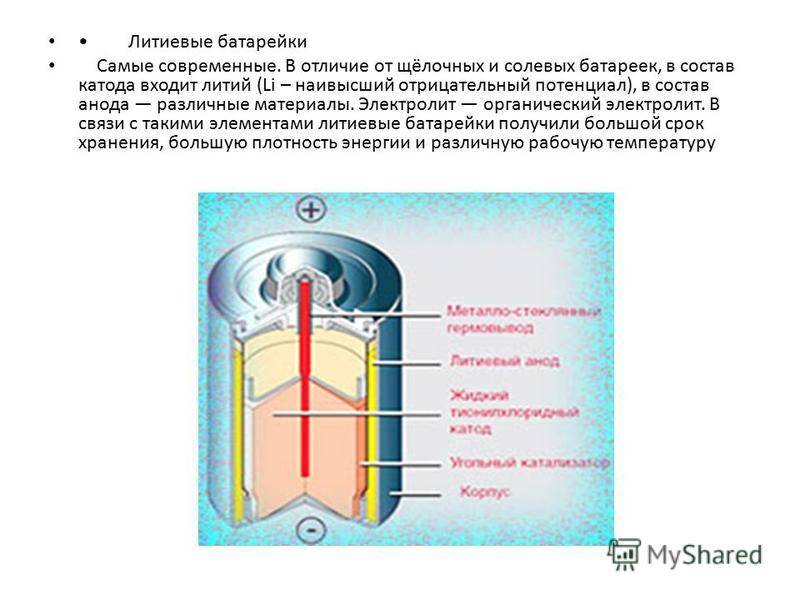
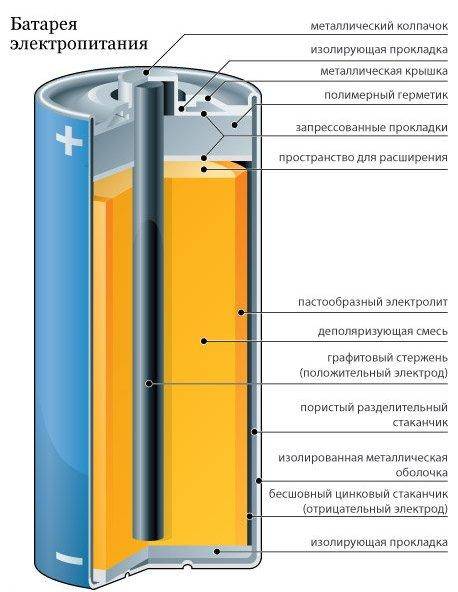
Что внутри батарейки?
Самые сложные элементы аккумуляторов мобильников находятся внутри корпуса. Можно изучить их конструкцию и основные функции. Кроме банки с ионами лития и сепаратора, конструкция оснащена контроллером.
Контроллер – это «мозги» батареи сотового, состоит из таких элементов:
- Резисторы (в схеме питания, защиты).
- Терморезистор.
- MOSFET-транзисторы.
- Микросхема.
- Конденсатор накопления.
Контроллер выполняет следующие функции:
- Контроль заряда. Аккумуляторы телефонов заряжаются постепенно. Первых 10% с невысокой скоростью, потом ускорение до 80%, и конечный этап – замедление. С высокой скоростью заряжается лишь «средняя часть» батарейки, такая особенность работы для снижения нагрузки.
- Защита от перезаряда. Ток от сети поступает, но при достижении напряжения в 4,2 В питание автоматически останавливается.
- Защита от разряда. Установлено и минимальное напряжение, на уровне, примерно в 2,9 В. Даже если процент упал до 0, и мобильный телефон выключился, в аккумуляторе остается небольшой запас. Если его не будет – потеряется полезная емкость.
- Ограничение тока. Напряжение не всегда стабильно, великие скачки или короткое замыкание – однозначно повредят батарею. Это плохо скажется на длительности срока эксплуатации. Ограничитель препятствует этому.
- Балансировка батареи. Это конструкция, состоящая из последовательных электронных элементов. Такая схема обеспечивает равномерный заряд разных частей. От функции зависит долговечность батарейки.
- Контроль за температурой. В каждой батарейке установлен терморезистор. Он контролирует температуру и при надобности защищает устройство от перегрева или переохлаждения.

Что называют аккумулятором
 Аккумулятором в самом общем значении этого понятия называется техническое приспособление, которое используется для накопления какого-либо вида энергии с целью её последующей равномерной отдачи в течение достаточно длительного периода времени (в отличие от конденсатора, который отдаёт накопленный заряд моментально). Конденсатор сохраняет непосредственно электрический заряд, в отличие от аккумулятора, который при зарядке преобразует электрическую энергию в энергию химической реакции, а когда будет работать под нагрузкой, превратит накопленную химическую энергию в электрическую.
Аккумулятором в самом общем значении этого понятия называется техническое приспособление, которое используется для накопления какого-либо вида энергии с целью её последующей равномерной отдачи в течение достаточно длительного периода времени (в отличие от конденсатора, который отдаёт накопленный заряд моментально). Конденсатор сохраняет непосредственно электрический заряд, в отличие от аккумулятора, который при зарядке преобразует электрическую энергию в энергию химической реакции, а когда будет работать под нагрузкой, превратит накопленную химическую энергию в электрическую.
Принцип работы аккумуляторной батареи заключается в том, что постоянно происходит химическая реакция между жидкостью-электролитом и металлическими пластинами-электродами. Единичные аккумуляторы очень слабы и не могут давать ток, достаточный для работы большинства устройств. Поэтому чаще всего они объединяются в аккумуляторные батареи, в которых используется последовательное или параллельное соединение отдельных элементов питания.
История обыкновенной батарейки
Слово «батарея», происходящее от французского слова «batterie», давно вошло в русский язык.
Название происходит от артиллерийской батареи, как исторически первого типа батарей. Впоследствии название стало употребляться для обозначения соединения однотипных предметов вообще.
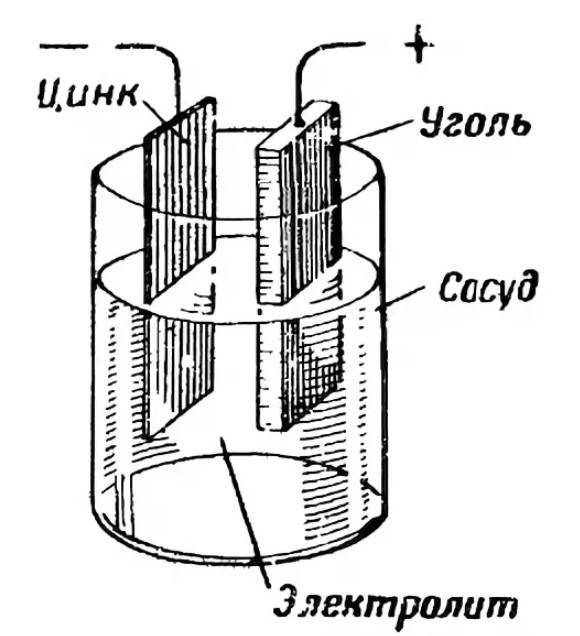
Официальное рождение батареи относят к 1800 г., когда итальянский физик Алессандро Вольта, основываясь на опытах итальянского врача и анатома Луиджи Гальвани, сделал устройство, получившее впоследствии название «вольтов столб». Сложив стопку высотой полметра из пластинок цинка, меди и войлока, смоченного раствором серной кислоты, Вольта, приложив руки к концам стопки, получил весьма чувствительный удар током. Так началась электрическая эра.
Изобретение Алессандро Вольта произвело фурор в обществе, Вольта осыпали почестями и наградами, его именем назвали единицу электрического напряжения. Свою долю славы получил и Луиджи Гальвани. В его честь электрохимический элемент, изобретенный Вольта, называется гальваническим.
Гальванические элементы делятся на два типа – первичные и вторичные.
Все батарейки являются первичными гальваническими элементами.
Вторичные гальванические элементы – элементы, в которых электрическая энергия от внешнего источника тока превращается в химическую энергию и накапливается, а затем, при необходимости, химическая энергия снова превращается в электрическую. Эти вторичные элементы называются аккумуляторами.
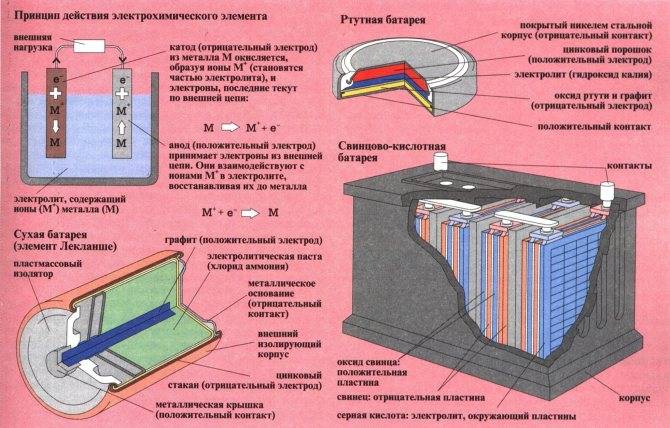
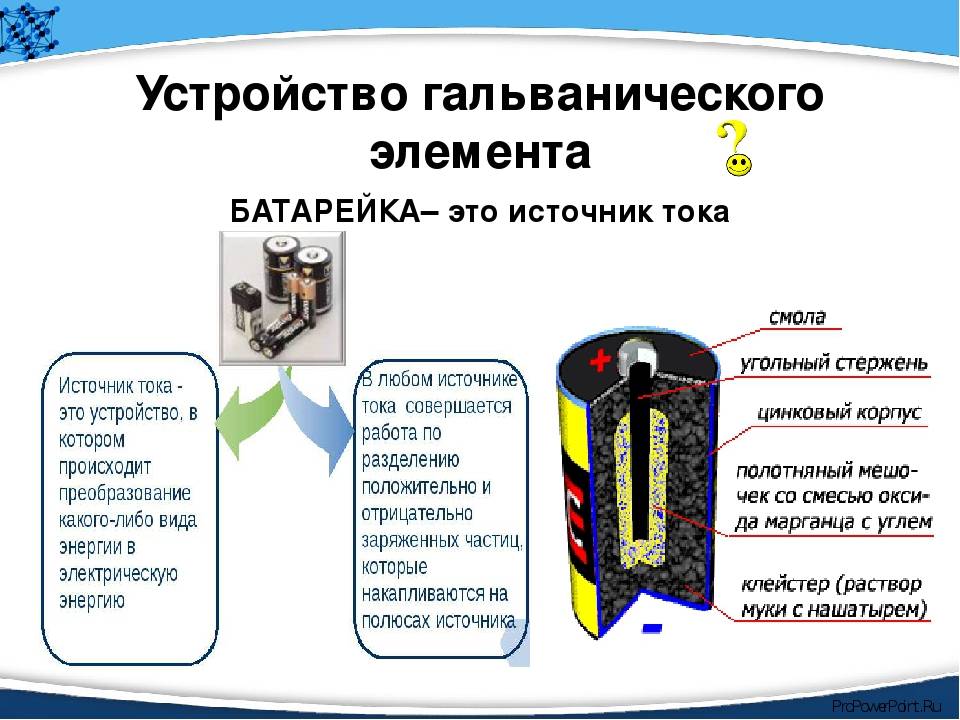
Одним из первых гальванических элементов, которым можно было пользоваться вне лабораторий, был изобретен Жоржем Лекланше в 1866 году.
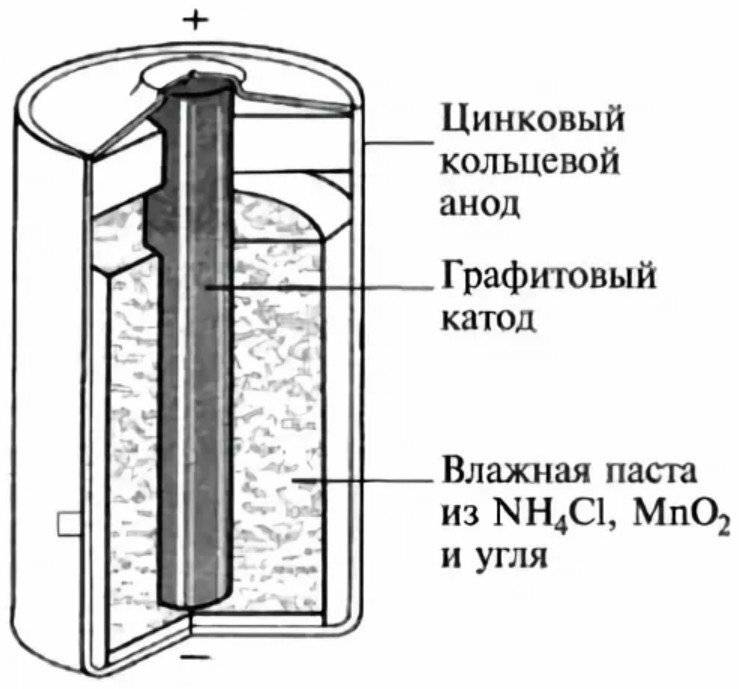
Конструкция имени Лекланше проста – цинковый анод, катод из диоксида марганца с углем, размещенные в электролите из хлорида аммония, т.е. соли аммония.
В течении некоторого времени элемент Лекланше претерпел изменения: цинковый анод стал делаться в виде цинкового стаканчика, в стаканчике размещен катод из смеси диоксида марганца и графита, в центре катода находится угольный стержень, являющийся токосъемником, катод окружен электролитом из хлорида аммония с добавкой хлорида цинка, только не в жидком виде, как у Лекланше, а в загущенном, в виде геля, из-за добавления крахмала и муки. Это необходимо для того, чтобы электролит не мог вытечь или высохнуть при хранении и эксплуатации элемента.
Элементы с загущенным электролитом получили название «сухие батареи».
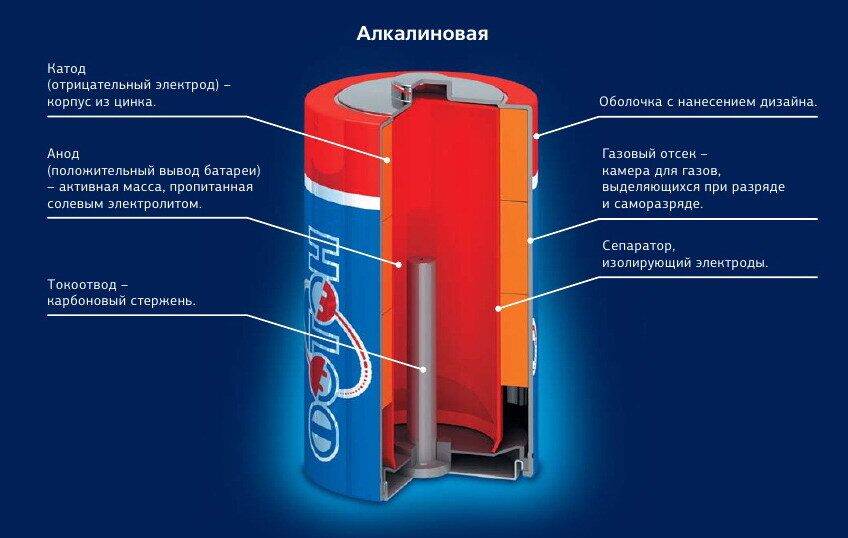
Одним из всплесков было появление щелочных батарей. Впервые щелочные батарейки выпустила компания Eveready (ныне Energizer) в 1959г. Принцип ее работы практически идентичен принципу работы солевой батареи – анод из цинка, катод из диоксида марганца, единственное отличие в составе электролита – он не из соли аммония, как в солевой, а из раствора щёлочи, обычно гидроксида калия. У щелочной батареи анод в виде пасты из цинкового порошка в смеси с электролитом находится внутри катода из смеси диоксида марганца с графитом.
Анод и катод разделены тонким сепаратором, пропитанным электролитом, и все это располагается в стальном корпусе. Получается, что если у солевого элемента корпус (-), а центральный токоотвод (+), то у щелочного элемента все наоборот, корпус (+), а центральный токоотвод (-).
Такая конструкция, разумеется, сделана не просто так. В солевых элементах при химической реакции расходуются все реагенты, составляющие этот элемент – анод, катод, электролит. А в щелочном элементе при химической реакции расходуется только анод и катод, электролит не расходуется. Поэтому электролита там совсем мало, и освободившееся место электролита заполнено увеличенным количеством анода и катода, что значительно увеличивает электроемкость щелочного элемента.
Форм-фактор распространенных гальванических элементов
Переработка батареек в России
Российский рынок батареек в последние годы развивается нестабильно: в 2015 и 2016 годах аналитики Discovery Research Group зафиксировали падение объема продаж — в первом случае всего на 1%, зато во втором — почти на четверть. В 2017-м в РФ было реализовано 816 млн элементов питания — при средней цене 43,2 руб. за штуку продажи в денежном выражении превысили 35 млрд руб. Сколько батареек добирается до переработки, эксперты не уточняют, однако для утилизации всего собираемого объема по состоянию на 2019 год фактически хватает мощностей одного завода — челябинского «Мегаполисресурса». Владелец и генеральный директор предприятия Владимир Мацюк пришел к идее подобного бизнеса во время занятий научной деятельностью. Третья глава его кандидатской диссертации была посвящена переработке редких видов отходов, и первой линией «Мегаполисресурса» стало оборудование для утилизации фиксажной жидкости. В этом элементе проявки фотографий содержится много серебра — из 1 л отходов можно получить до 4 г металла.
Со временем рост популярности цифровой фотографии сделал бизнес нерентабельным и мощности завода перепрофилировались под переработку офисной техники и другой электроники. На сей раз металлы «добывались» с печатных плат — в основном речь шла о золоте, серебре и меди.
До батареек Мацюк «добрался» в 2012-м. «Я выступал с докладом на форуме в Челябинске, и меня спросили: А батарейки вы сможете переработать? — вспоминал предприниматель в интервью RecycleMag. Задавшие вопрос активисты тут же передали ему 100 кг «сырья». Батарейки оказались одним из простейших для переработки товаров. Технология умещается в два этапа: измельчение металлической оболочки и сортировка солей цветных металлов. Последние можно использовать для производства новых элементов питания.
Мацюк быстро наладил производственный процесс и принялся активно экспериментировать с материалами, которые приносили «разные люди и организации». Тогда же на фоне роста популярности у населения «зеленых» потребительских привычек раздельно собирать батарейки стали крупные торговые сети. Уже спустя несколько месяцев к «Мегаполисресурсу» обратились IKEA и MediaMarkt — обе компании готовы были собирать и доставлять на завод партии элементов питания. Вскоре к ним присоединился «Вкусвилл». Также среди партнеров завода — один из крупнейших мировых производителей батареек Duracell. В декабре 2017-го на предприятии открыли новую линию, предназначенную исключительно для батареек. В технологии производства при этом ничего кардинально не поменялось — просто раньше элементы питания перерабатывали в «перерывах» между утилизацией электротехники.
Переработка батареек в России остается в зачаточной стадии — и монополия «Мегаполисресурса» тому яркое доказательство: объемы, достаточные для загрузки мощностей других предприятий, просто не собираются, констатировал Мацюк в интервью РБК. По данным СПАРК, в 2018-м выручка завода превысила 7 млн руб., а убыток составил 1,5 млн руб.
Что такое свинцово-кислотный аккумулятор
Свинцовый аккумулятор – такой тип химического источника тока, который основан на реакции свинца и серной кислоты. Его изобретателем считается Гастон Планте, а первое появление датируется 1859-1860 годами. В 1878 году устройство аккумулятора было усовершенствовано изобретателем Камиллом Фором, который предложил наносить на пластины свинцовый сурик – красно-оранжевый порошок, представляющий собой ортоплюмбат свинца. В том же веке Николай Николаевич Бенардос – русский инженер и изобретатель – покрыл пластины батареи губчатым свинцом, добившись увеличения мощности.

Чтобы узнать, какой процесс происходит в аккумуляторе во время его работы, необходимо подробно рассмотреть его устройство. Конструкция современного кислотного аккумулятора включает в себя:
- корпус из кислотоупорного материала;
- электролит, представляющий собой раствор серной кислоты в дистиллированной воде;
- анодные – положительные – решетчатые свинцовые пластины, в ячейках которых запрессован порошок диоксида свинца;
- катодные – отрицательные – решетчатые свинцовые пластины, в ячейках которых – губчатый свинец;
- сепараторы, выполненные из пористого, не контактирующего с кислотой материала и предназначенные для разделения положительно и отрицательно заряженных пластин и предупреждения короткого замыкания между ними
- крышку (обычно встречается в переносных батареях), для достижения герметичности упаковки залитая мастикой;
- бареток, соединяющих одноимённые пластины и служащих в качестве токоотвода;
- крепёжные и соединительные элементы.
Принцип действия свинцового аккумулятора заключается в следующем. Положительные и отрицательные электроды опущены в электролит, и при подключении источника тока к внешней цепи оксид свинца вступает в химическую реакцию с серной кислотой. По мере разрядки батареи на аноде окисляется свинец, а на катоде происходит процесс восстановления диоксида свинца. Также при уменьшении заряда в АКБ плотность электролита снижается из-за расхода серной кислоты и выделения воды. Но стоит учитывать, что в процессе зарядки устройства запускаются обратные процессы.
| Кислотные аккумуляторные батареи | |
| Классификация | Вид |
| По конструкции анодов | · Поверхностные · Панцирные, трубчатые · Стержневые намазные · Решётчатые |
| По агрегатному состоянию электролита | · Жидкостный · Гелевый · Абсорбированный |
| По возможности обслуживания | · Обслуживаемый · Необслуживаемый · Малообслуживаемый |
| По назначению | · Стартерные · Тяговые · Промышленные |
Параметры батареи, тип, страну-производителя и прочую необходимую информацию пользователь может узнать через маркировку, не прибегая к техническому паспорту устройства.
В источниках тока, сделанных в России, обозначение происходит согласно ГОСТ, и шифр обязательно включает в себя (по порядку):
- количество банок в корпусе;
- обозначение типа, например, «СТ» – стартерная;
- ёмкость, измеряемая в А∙ч;
- материал и особенности конструкции.
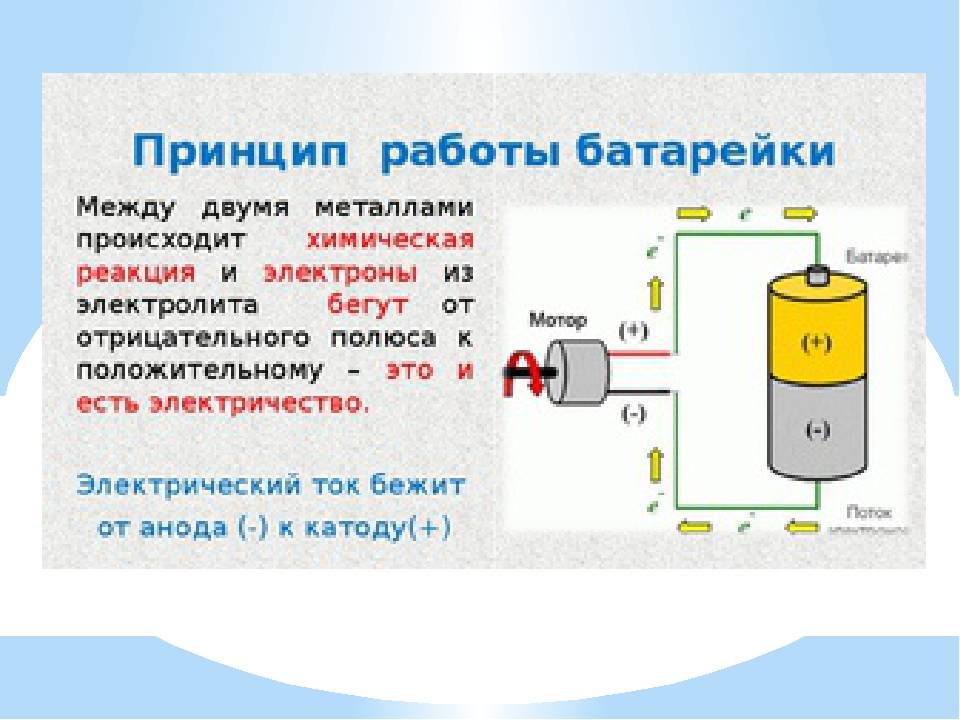
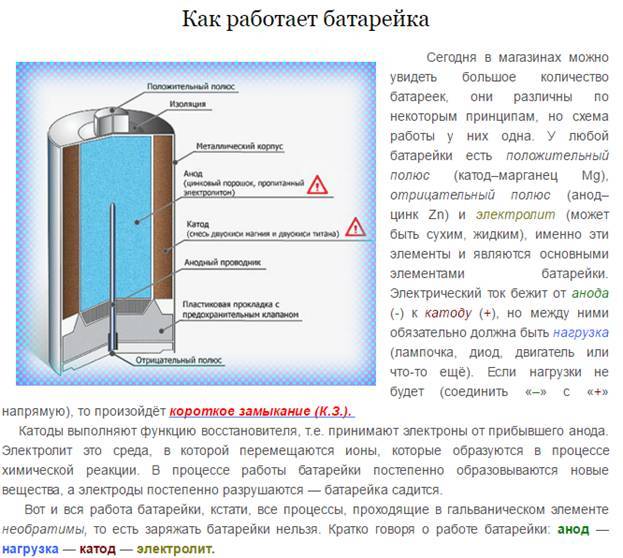
Как работает батарейка
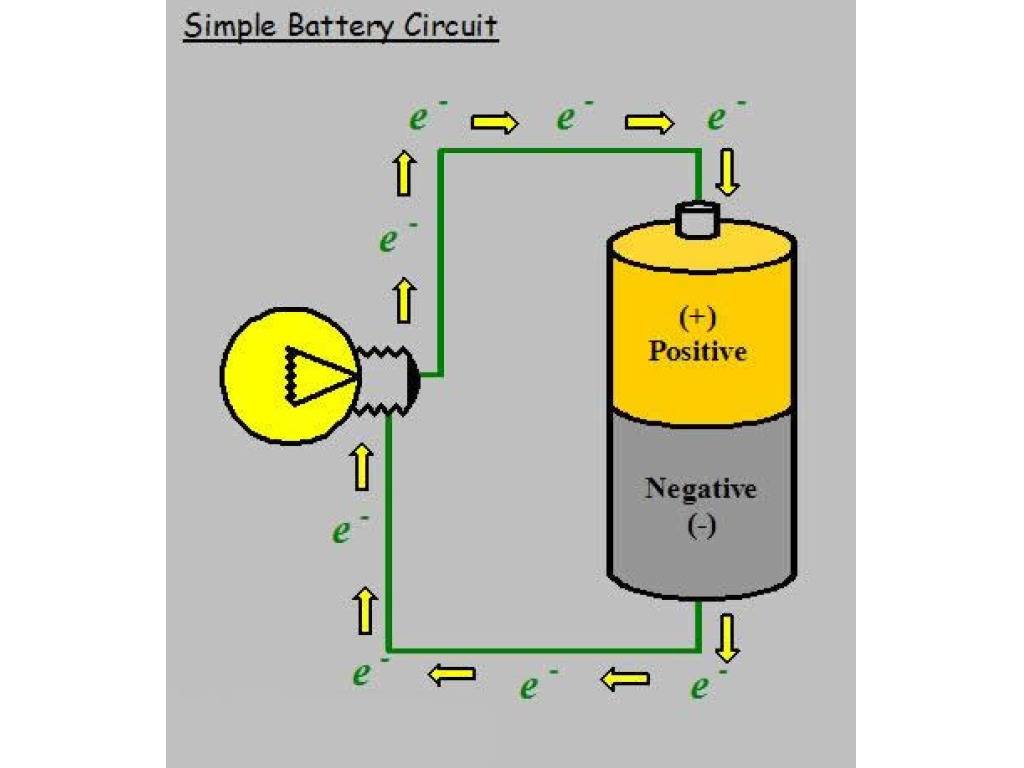
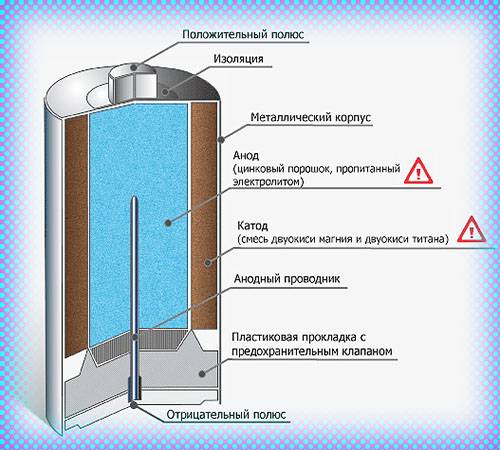 Сегодня в магазинах можно увидеть большое количество батареек, они различны по некоторым принципам, но схема работы у них одна. У любой батарейки есть положительный полюс (анод–цинк Zn), отрицательный полюс (катод–марганец Mg) и электролит (может быть сухим, жидким). Именно эти составляющие и являются основными элементами батарейки. Электрический ток бежит от анода (+) к катоду (—), но между ними обязательно должна быть нагрузка (лампочка, диод, двигатель или что-то ещё). Если нагрузки не будет (соединить «–» с «+» напрямую), то произойдёт короткое замыкание (К.З.)
Сегодня в магазинах можно увидеть большое количество батареек, они различны по некоторым принципам, но схема работы у них одна. У любой батарейки есть положительный полюс (анод–цинк Zn), отрицательный полюс (катод–марганец Mg) и электролит (может быть сухим, жидким). Именно эти составляющие и являются основными элементами батарейки. Электрический ток бежит от анода (+) к катоду (—), но между ними обязательно должна быть нагрузка (лампочка, диод, двигатель или что-то ещё). Если нагрузки не будет (соединить «–» с «+» напрямую), то произойдёт короткое замыкание (К.З.)
Катоды выполняют функцию восстановителя, т.е. принимают электроны от прибывшего анода. Электролит это среда, в которой перемещаются ионы, которые образуются в процессе химической реакции. В процессе работы батарейки постепенно образовываются новые вещества, а электроды постепенно разрушаются — батарейка садится.
Вот и вся работа батарейки, кстати, все процессы, проходящие в гальваническом элементе, необратимы, то есть заряжать батарейки нельзя. Кратко говоря о работе батарейки: анод — нагрузка — катод — электролит.
Электролит изначально изготовляли в жидком виде, но это неудобно, так как при переворачивании батарейки она просто не работала. Из-за этого электролит стали загущать, превращать его в сухой вид.
Применение
Различные виды могут применяться по-разному, зависит это от их основных конструктивных свойств и характеристик:
- Элементы питания с твердым электролитом используют в устройствах с малым значением потребляемого тока. Например, часы фонарики с малой мощностью, а также пульты дистанционного управления.
- Щелочные батарейки применяют в электротехнике с повышенным значением тока, к ним можно отнести различные камеры и магнитофоны, а также игрушки с электродвигателем.
- Источники питания с серебряными электродами способны обеспечить электроэнергией в калькуляторах, переносных инструментах и аппаратах для улучшения слуха.
- Литиевые батарейки используют в портативной электронике, где необходимо стабильное значение емкости и потребляемого тока.
Что происходит с точки зрения химии?
К примеру, в стеклянную емкость нальем раствор серной кислоты и поместим туда стержень, выполненный из цинка. На поверхности данного стержня имеются положительно заряженные ионы. А вокруг этого цинкового объекта, в растворе, скапливаются отрицательные ионы вещества. У раствора имеются силы притяжения, которые с легкостью отрывают ионы цинка. В результате жидкость получает положительный заряд, а цинковая пластина или стержень отрицательный.
Из физики известно, что разность потенциалов равна напряжению. Отсюда и возникает электрический ток. Когда происходит контакт кислотного раствора и металла, на границе образуется электрическое поле. В момент его появления химическая энергия превращается в электрическую. Таков принцип работы батареи.
Через некоторое время ресурс батареи будет истощен. Все зависит от того, где и как используется источник питания. Например, если от него работает фонарик, то при умеренном использовании 2-х батарей на 1,5 вольта каждая, хватит на 1 месяц. Но если вставить эти же самые батарейки в электрическую машинку, она будет работать несколько часов. В результате всего этого можно сделать вывод что чем больше нагрузка, тем быстрее разрядиться батарейка.
О батарейке на материнской плате
Раньше в системные блоки для хранения параметров BIOS устанавливалась энергозависимая память CMOS RAM. Батарейка на материнской плате нужна была для хранения персональных настроек, позволяющих включить компьютер, запустить операционную систему. Энергопотребление в автономном режиме было незначительным, элемента питания хватало на несколько лет работы, что примерно соответствовало сроку службы оборудования. Когда срок службы ИП подходил к концу, на экран выводилось уведомление об ошибке, требующее от пользователя провести замену.
С прогрессом в стационарные компьютеры, лаптопы стаи устанавливать материнки с энергонезависимой памятью. После отключения от источника питания, при разряде основного АКБ, персональные параметры, информация были в сохранности.
Как работает батарейка — видео
Химическая реакция в батарейке, к которой подключен потребитель:
- Свободные электроны поступают в батарею через положительную клемму.
- Они соединяются с оксидом марганца и молекулой воды на катоде, которая высвобождает ион гидроксида в электролит.
- Ион гидроксида проходит через сепаратор и соединяется с атомом цинка, образуя гидроксид цинка, и при этом высвобождаются электроны и молекула воды.
- Электроны хотят попасть в область с меньшим количеством электронов, так как положительная клемма имеет меньше электронов, поэтому они будут течь по проводу, чтобы достичь ее.
- Химическая реакция повторяется снова и снова до тех пор, пока не иссякнет ресурс батарейки.
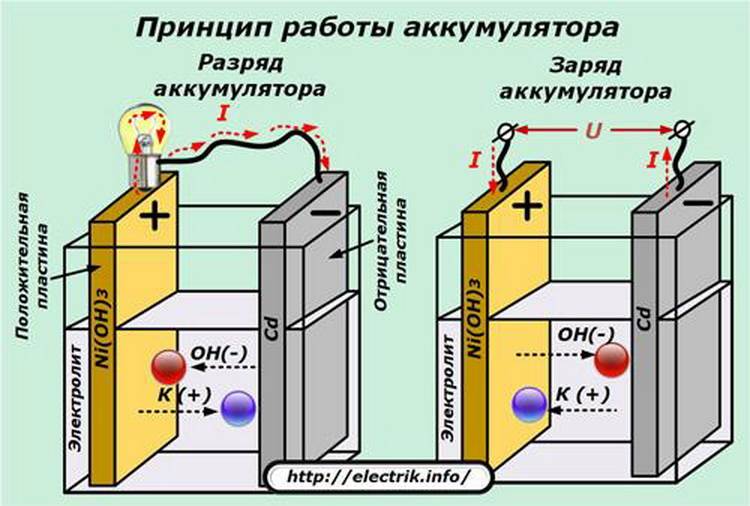
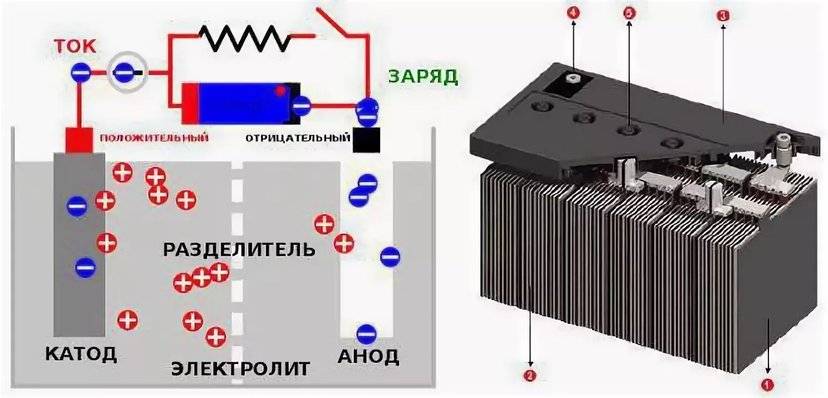
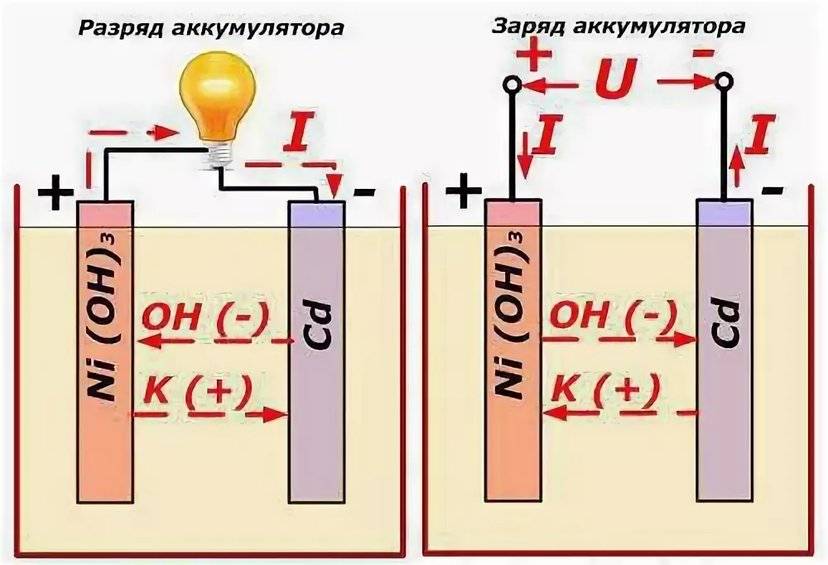
Как работает аккумулятор (АКБ) при разряде
В момент, когда к электродам подключена нагрузка в виде лампочки, создается замкнутая электрическая цепь, через которую протекает ток разряда. Его формированию способствует движение электронов в металлических частях и анионов с катионами в электролите.
Этот процесс условно показан на схеме с никель-кадмиевой конструкцией электродов.
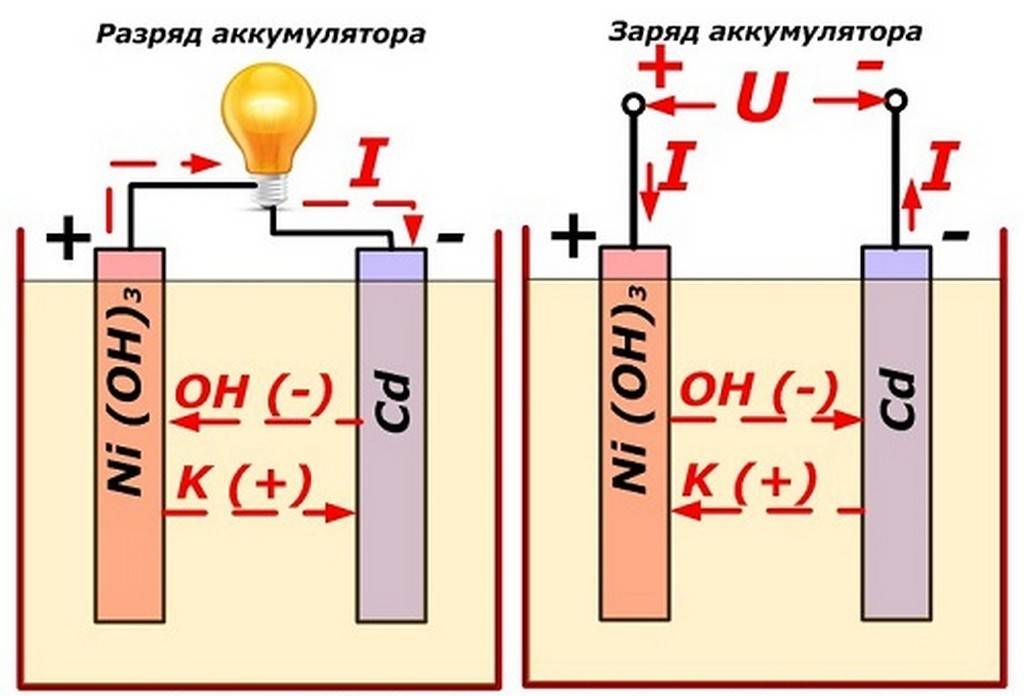 Заряд и разряд аккумулятора
Заряд и разряд аккумулятора
В данном примере в качестве материала положительного электрода используют окислы никеля с добавками графита, которые повышают электрическую проводимость. Металлом отрицательного электрода работает губчатый кадмий.
Во время разряда частицы активного кислорода из окислов никеля выделяются в электролит и направляются на отрицательные пластины, где окисляют кадмий.
 Общее устройство и маркировка аккумуляторных батарей
Общее устройство и маркировка аккумуляторных батарей
Выбор источника питания
Для правильного выбора элементов питания необходимо обратить внимание на следующие факторы:
В аппаратах и оборудовании какого вида он будет применяться.
Электролит какого состава используется в конструкции.
Стоимость батарейки, иногда более выгодно приобрести несколько дешевых, чем один очень дорогой.
Каждый элемент питания на корпусе имеет маркировку, по которой можно определить вид и состав источника питания.
Необходимо ориентироваться по условиям окружающей среды в процессе эксплуатации.
Рекомендуется приобретать источники питания, произведенные сравнительно недавно, так как с течением времени емкость может понижаться.
Перед покупкой следует обратить внимание на целостность упаковки и самого корпуса элемента.
Батарейка должна конструктивно соответствовать своему посадочному месту в электроприборе.
Правильный выбор и соблюдение требований к безопасной эксплуатации позволит продлить работу любого элемента питания. Для определенных видов техники необходим свой вид батарейки.
Корпус для батареек и из чего он сделан?
Такая деталь батарейки как корпус играет очень значительную роль. По сути она удерживает все ее содержимое и предотвращает от распада деталей в разные стороны.
В каких батарейках цинковый корпус?
Многих интересует данный вопрос и это не спроста. Цинк можно использовать для различных экспериментов. Или же его можно просто продать. Цинковым корпусом обладают солевые источники питания. Обычно на них стоит надпись что они солевые.
Последнее время встречаются элементы питания, поверхность которых сделана из железа, жести. Это связано с тем что находится внутри источников энергии. Для повышенной прочности и защиты требуется именно такой кожух.
Из чего состоит корпус пальчиковой батарейки?
Он имеет простое устройство и состоит из нескольких частей:
- Верхняя
- Нижняя
- Боковая овальная
- Маркировка
Но под корпусом порой люди имеют ввиду отсек куда вставляются элементы питания. Например, по типу такого:

Корпус для батареек xbox 360
Он выглядит по типу так:

Можно изготовить корпус для батареек своими руками. Но на это нужно время. Ниже в видео представлено как это можно сделать из подручных средств.
Примерный химический состав всех батареек
В каждом типе энергетических накопителей содержатся разные химические элементы. Вот химические элементы, встречающиеся в источниках энергии:
- Никель
- Кадмий
- Свинец
- Ртуть – сейчас уже редко используется.
- Литий
- Цинк
- Марганец
- Алюминий
- Железо
Таким образом по составу элементы питания выглядит как-то так! Но устройство энергетического элемента не может включать в себя сразу все эти вещества.
В итоге из чего сделаны батарейки теперь понятно.
Основные характеристики АКБ
Ёмкость
Данная характеристика обозначает способность батареи отдавать электроэнергию. Расчёт этого значения выполняется умножением показателей силы тока и времени. Единица измерения А/ч. Ёмкость батареи имеет зависимость от конструктивных особенностей (материал, взятый при производстве электродов и сепараторов, их качество, размер и пр.), кроме того от особенностей рабочего раствора (температурный показатель и значение плотности, объем заряженности и режим разряда). Показатель ёмкости существенно понижается при низкой температуре и небольшой плотности рабочей смеси.
Номинальная ёмкость выражает кол-во отдаваемой электрической энергии. Данное значение замеряется при соблюдении следующих условий:
- АКБ должна быть заряжена на 100%.
- Значение тока равняется 1/20 ёмкости при беспрерывном разряде в течение 20ч.
- Электролит должен иметь температуру 25C.
- Значение напряжения на выходе должно быть не менее 10,5В.
Ток холодной прокрутки (ТХП)
Данная характеристика необходима для определения пусковых свойств батареи при низкой температуре. Оно измеряется при минус 18C с полностью заряженной батарей.
Показатель ТХП не должен снижааться за отметку заданного показателя в течение установленного кол-во времени. Чем больше показатель ТХП, тем проще будет заводиться мотор в зимний период.
Коэффициент заряда (КЗ)
При заряде батареи необходим значительный объем энергии. Он гораздо больше объема, который АКБ отдает. Это связано с потерями в процессе нагрева и сопутствующими химреакциями.
Для полного заряда батареи необходимо 105-110%% электрической энергии, взятой с АКБ.
Напряжение гальванических элементов
Это напряжение между плюсовыми и минусовыми отводами гальванических элементов. На показатель влияет концентрация, а также температура кислоты в рабочей смеси.
У стандартной батареи любой гальванический элемент имеет показатель 2В.
Номинальное напряжение (НН) и напряжение на выводе
В соответствии с действующими стандартами показатель НН одного элемента АКБ равняется 2В. Поскольку элементы соединены последовательным способом, общий показатель напряжения равняется сумме значений всех значений. Отсюда получается общее напряжение батареи 12В.
Напряжение на выводе — показатель напряжения, которое измеряется на отводах полюсов АКБ.
 Маркировка АКБ
Маркировка АКБ
Напряжение газовыделения
Показатель напряжения заряда, превышение которого провоцирует выделение газа. Данный показатель связан с температурным значением. Для любого элемента он равняется 2,4В. Значит, вся АКБ имеет показатель 14,4В.
Превышение данного показателя ведет к разложению дистиллята, содержащегося в рабочем растворе. Это способствует образованию водорода и кислорода, а при их смешении образуется взрывоопасный газ.
Напряжение холостого хода (НХХ)
НХХ также называют напряжением покоя – это напряжение на отводах при отсутствии нагрузки. После заряда/разряда аккумулятора НХХ меняет показатель.
Потеря воды
При показателе напряжения выше 14,4В дистиллят электролита аккумулятора быстро разлагается и улетучивается. Скорость данного процесса зависит от температурного режима.
Показатель уровня рабочего раствора понижается, процент содержания кислоты возрастает, а период службы АКБ становится меньше. Из-за этого увеличивается вероятность образования искры, что может спровоцировать взрыв батареи.
Отвод газа
Для отвода газов, образованных при химреакциях, в батарее имеется газоотвод. Это обеспечивает направленный отвод газа в определенное место. Вывод газа осуществляется с разных сторон (плюс/минус) — это зависит от места его нахождения в батарее. В некоторых модификациях АКБ предусмотрено 2 отверстия для отвода газа — на обеих сторонах вывода.
Саморазряд
Процесс, вызванный химреакциями, происходящими внутри батареи. Он происходит даже если к аккумулятору нет подключений внешних потребителей. Показатель зависит от температурного режима и технологических процессов, применяемых при производстве батареи.
Для сведения значения к минимуму в производстве электродов не используют сурьму для сплава со свинцом, заменяя ее кальцием. Это гарантирует наименьшее значение саморазряда в ходе старения. В соответствии с установленными нормативами саморазряд АКБ равен ориентировочно 3% в месяц (0.1% в день).
 АКБ в системе автомобиля
АКБ в системе автомобиля
Ядерная батарейка на углероде 14 работающая 100 лет
У данной атомной батарейке по сравнению с другими радиационными источниками энергии имеются следующие преимущества:
- Дешевизна.
- Экологическая чистота.
- Долгий срок работы до 100 лет.
- Низкая токсичность.
- Безопасность.
- Способна работать в экстремальных температурных условиях.
Радио активный изотоп углерод 14 имеет период полураспада 5700 лет. Он абсолютно не токсичен и имеет низкую стоимость.
Активную работу по модернизации ядерной батарейки ведут не только США и Россия, но и другие страны! Исследователи научились наращивать пленку на карбидной подложке. В результате чего подложка подешевела в целых 100 раз. Такая структура устойчива к радиации, а это делает данный энергетический источник безопасным и долговечным. Применяя карбид кремния в ядерные батареи можно добиться ее работы при температуре в 350 градусов Цельсия.
Таким образом ученым удалось создать атомную батарейку своими руками!
Заключение
Теперь вы знаете, как работает аккумулятор. Его роль в работе приборов трудно оспорить. Данный источник энергии применяться почти во всех отраслях. Что доказывает его значимость и необходимость знаний о принципе работы АКБ. А также ее внутреннем содержимом. Аккумуляторы широко используются в автомобилях, разнообразных электроприборах, кондиционерах, мультимедийных центрах. Там, где, генераторы не всегда справляются с обеспечением их энергией. И тогда в «игру» вступает АКБ, которая кроме подпитки энергией еще и выполняет основную функцию, обеспечивая электроэнергией стартер двигателя. Водителю необходимо знать, как устроен аккумулятор. Ведь в нужное время придется устранять сбои в работе источника энергии
К тому же, важно иметь представление о назначении и видах аккумулятора, чтобы правильно использовать ресурс, подобрать батарею к условиям эксплуатации и автомобилю
 Как работает аккумулятор (АКБ)
Как работает аккумулятор (АКБ)